
中大新聞網訊(通訊員周良)近日,中山大學生命科學學院崔雋教授課題組在《Nature Cancer》上發表研究論文,開發出新型抑制劑,為癌癥免疫治療提供了全新策略。
鐵死亡(Ferroptosis)是一種由脂質過氧化引發的細胞死亡方式,近年來被證實是癌癥免疫治療的關鍵機制之一。盡管免疫細胞可通過誘導腫瘤細胞鐵死亡來殺傷腫瘤,但多數腫瘤細胞能通過未知機制抵抗這一過程,導致治療失效。
崔雋教授團隊經過研究發現,棕櫚酰基轉移酶zDHHC8在黑色素瘤、結直腸癌、胰腺癌等多種腫瘤中高表達,且與CD8+ T細胞浸潤呈負相關。zDHHC8能對鐵死亡防御核心蛋白GPX4進行棕櫚酰化修飾,幫助其在鐵死亡誘發時錨定到脂質過氧化活躍的內質網膜等細胞器膜上,高效清除有害代謝產物,從而幫助腫瘤細胞抵抗鐵死亡。基于這一發現,崔雋教授團隊通過高通量篩選找到了一種小分子化合物PF-670462。在體外和體內實驗中,PF-670462顯著增強了腫瘤細胞對鐵死亡的敏感性,并在腫瘤模型中顯著促進CD8+ T細胞浸潤。
“這一發現不僅揭示了腫瘤免疫逃逸的新機制,更提供了克服耐藥性的雙贏策略—既能提升免疫細胞對腫瘤的殺傷效果,又避免了對免疫系統的損傷。”崔雋教授說。
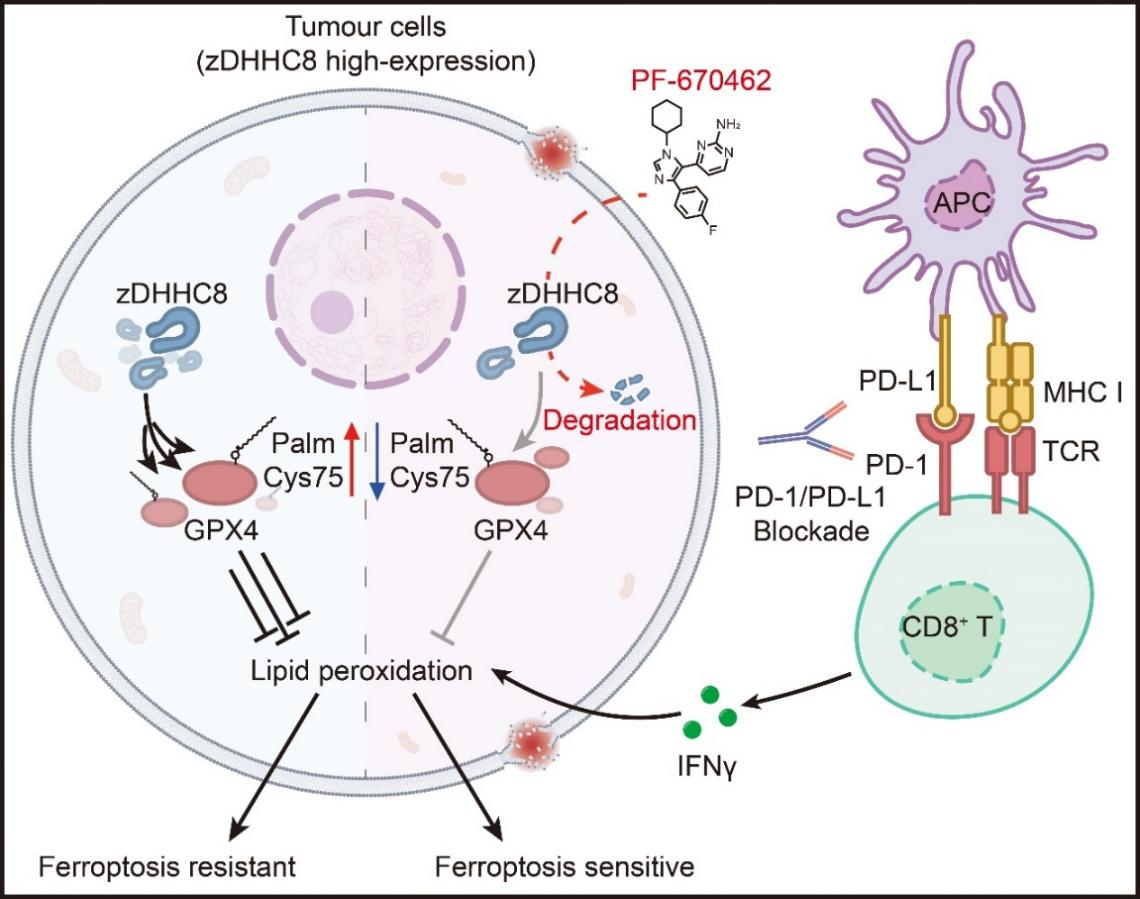
靶向zDHHC8-GPX4棕櫚酰化信號軸,增強腫瘤細胞的鐵死亡敏感性,提升抗腫瘤免疫治療效果。
論文鏈接:https://www.nature.com/articles/s43018-025-00937-y