
自然界存在許多性能優(yōu)異的跨膜蛋白通道可以高速度和高選擇性使脂質(zhì)雙層上的陽離子進行傳輸。受自然界的啟發(fā),科學(xué)家們開發(fā)了模擬人工離子通道的簡化模型,以研究跨膜傳輸?shù)尿?qū)動因素及其在藥物、生物材料開發(fā)方面的潛在應(yīng)用。其中自然鉀離子通道蛋白除了鉀離子外不允許其他陽離子通過,呈現(xiàn)高的運載鉀離子速率和選擇性。這種高度選擇性是自然通道蛋白運輸效果的重要決定因素,因此,吸引了很多化學(xué)家的研究興趣。在已經(jīng)報道的研究結(jié)果中,很多報道的人工鉀離子通道并未重視K+/Na+的高選擇性通過問題。通常來說,金屬陽離子選擇性是由陽離子脫水損耗的能量與離子得到補償?shù)哪芰勘戎禌Q定的。
我校化學(xué)學(xué)院Lehn功能材料研究所超分子化學(xué)與材料方向外籍專家Mihail Barboiu教授長期致力冠醚衍生物協(xié)助離子傳輸?shù)姆派瘜W(xué)研究,近期報道了一系列高選擇性鉀離子通道(J. Am. Chem. Soc. 2006, 128, 9541-9548; Angew. Chem. Int. Ed. 2015, 54, 14473-14477; J. Am. Chem. Soc. 2016, 138, 426-432; J. Am. Chem. Soc. 2017, 139, 3721-3727;Angew. Chem. Int. Ed., 2018, 57, 10520-105)。
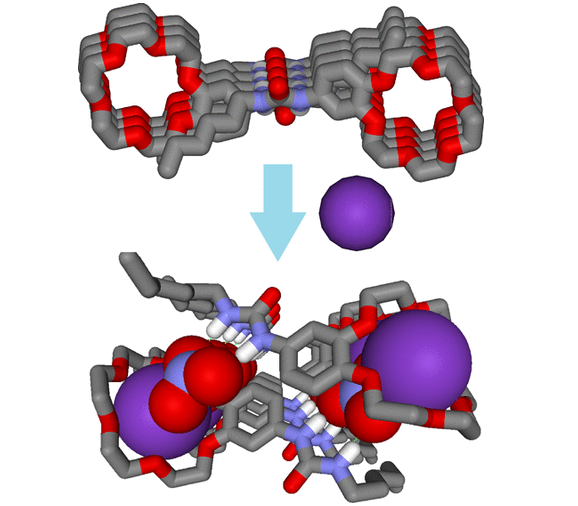
冠醚衍生物通過自身攜帶的大環(huán)識別位點,高選擇性地與鉀離子配位,協(xié)助鉀離子傳輸
結(jié)合上述研究及國內(nèi)外同行研究成果,Mihail Barboiu教授總結(jié)了過去10年來跨膜傳輸鉀離子的人工通道蛋白的最新進展,綜述了人工鉀離子通道或運輸載體選擇性設(shè)計及其功能特性,特別是選擇性運輸鉀離子的功能設(shè)計,有助于進一步探究活性結(jié)構(gòu)作為“過濾器”或“門控”蛋白在離子傳輸過程中的動態(tài)過程。綜述指出人工鉀離子通道一般具有以下特征:(i)鉀離子結(jié)合的大環(huán)識別位點。配位后大環(huán)通道獲得的能量可以補償鉀離子脫水后能量損耗。即使體系中存在過量的Na+離子,大環(huán)通道也只識別K+離子。從機理上看,該識別系統(tǒng)具有協(xié)同動態(tài)效應(yīng),K+離子的增加也協(xié)同驅(qū)使著大環(huán)通道對鉀離子的選擇性增大;(ii)能夠?qū)崿F(xiàn)分子間自組裝的氫鍵供體與受體;(iii)具有可以嵌入疏水雙層膜結(jié)構(gòu)的疏水鏈。
該綜述分析和總結(jié)了該類材料體系中跨膜傳輸鉀離子的機理與機制;總結(jié)了人工設(shè)計自組裝高選擇性鉀離子通道的特征,并對比了一系列的人工鉀離子通道單晶結(jié)構(gòu)特點及其跨膜運輸?shù)奶攸c。同時,他們還分析探討了該領(lǐng)域的未來發(fā)展前景與挑戰(zhàn)。相關(guān)研究成果以“Encapsulation versus Self-Aggregation toward Highly Selective Artificial K+ Channels”為題發(fā)表在Account of chemical research上。